Lo Studio Clinico Assistenziale: Un Percorso Complesso per l'Innovazione Terapeutica
La ricerca clinica, pilastro fondamentale del progresso medico, rappresenta un intricato ecosistema di collaborazione e responsabilità, in cui diverse figure professionali operano sinergicamente per garantire la sicurezza, l'efficacia e l'affidabilità di nuove terapie. Dalle autorità regolatorie ai comitati etici, dagli sponsor agli sperimentatori, ogni attore riveste un ruolo cruciale nel complesso percorso che porta una potenziale innovazione dal laboratorio al paziente. Comprendere appieno questo processo è essenziale non solo per gli addetti ai lavori, ma anche per i cittadini, affinché possano prendere decisioni informate sulla propria partecipazione a studi clinici, contribuendo così al bene comune e al progresso scientifico.

Le Figure Chiave e le Loro Responsabilità
La conduzione di una sperimentazione clinica richiede una stretta collaborazione tra molteplici figure specifiche, ognuna con una chiara job description che ne definisce l'ambito di azione e le responsabilità, sia individuali che condivise. Tra queste, spiccano le seguenti:
- Autorità Regolatoria (o competente): Organismo con il potere di emanare disposizioni normative. Insieme ai comitati etici, revisiona i dati degli studi clinici e garantisce la sicurezza dei soggetti, del prodotto in sperimentazione e dello sperimentatore durante tutte le fasi dello studio. La sua profonda conoscenza del protocollo, del prodotto e delle GCP è imprescindibile.
- Comitato Etico (CE): Un organo indipendente, composto da personale sanitario e non, il cui compito primario è tutelare i diritti, la sicurezza e il benessere dei partecipanti allo studio. Fornisce inoltre una garanzia pubblica di tale tutela, valutando attentamente la serietà, la correttezza scientifica, etica e applicativa di ogni protocollo di studio.
- Sponsor: La persona, società o istituzione che si assume la responsabilità di avviare, gestire e/o finanziare una sperimentazione clinica. Negli studi profit, si tratta tipicamente di aziende farmaceutiche o biotecnologiche.
- Promotore: Una struttura, ente, istituzione pubblica o privata, fondazione, associazione scientifica o di ricerca, che si assume la responsabilità di avviare, gestire e/o finanziare la ricerca clinica.
- Principal Investigator (PI): Un medico qualificato, responsabile dell'esecuzione clinica in un determinato centro sperimentale. È garante del rispetto delle Norme di Buona Pratica Clinica (GCP) e della normativa vigente, ed è il responsabile ultimo del benessere dei pazienti arruolati. Può nominare un co-sperimentatore per delegare funzioni.
- Co-Principal Investigator (Co-PI): Designato e supervisionato dal PI, può essere delegato a svolgere procedure e attività previste dal protocollo, o a prendere decisioni connesse allo studio.
- Study Coordinator (SC): Figura di coordinamento tra tutti i partecipanti allo studio, assicura che la ricerca sia condotta in accordo con le GCP.
- Data Manager (DM): Responsabile della gestione dei dati clinici, dalla raccolta al trattamento, all'elaborazione e al trasferimento finale ai centri statistici.
- Sub Investigator (SI): Sperimentatori delegati dal PI a condurre specifiche attività clinico-assistenziali e terapeutiche previste dal protocollo.
- Research Nurse (RN): Infermiere con il compito di coordinare lo studio a livello di reparto, fungendo da consulente per il personale sanitario riguardo all'assistenza dei pazienti inclusi nel protocollo.
- Contract Research Organization (CRO): Società specializzata che stipula accordi per gestire parti o la totalità delle competenze relative a una sperimentazione clinica, offrendo servizi che spaziano dallo sviluppo del prodotto al monitoraggio, alla farmacovigilanza e al supporto regolatorio.
- Clinical Research Associate (CRA/monitor): Responsabile del monitoraggio, garantisce che la sperimentazione sia condotta e documentata in modo appropriato secondo le GCP.
- Biostatistico: Supporta il ricercatore nella stesura del piano di analisi statistica, nel calcolo del campione e nella definizione dei metodi statistici, oltre ad eseguire le analisi dei dati.
La Struttura della Ricerca Clinica: Dal Concetto alla Pratica
La ricerca clinica, per sua natura, si basa su un esperimento scientifico volto a produrre informazioni valide e generalizzabili. L'etica della ricerca impone norme ancora più stringenti rispetto all'etica medica, distinguendola sulla base di un'ipotesi verificabile, la necessità di conclusioni valide e lo sviluppo di conoscenze generalizzabili. La valutazione etica considera il disegno scientifico dello studio, gli obiettivi, i criteri di arruolamento, il rapporto rischio/beneficio e l'uso delle risorse, sempre nel rispetto dei principi di dignità umana, beneficità, non maleficità ed equità.
Tipologie di Studi Clinici: Osservazionali e Sperimentali
La metodologia epidemiologica clinica classifica gli studi clinici in due grandi gruppi:
- Studi Osservazionali: Utili per descrivere cause e conseguenze delle malattie, identificare fattori che ne modificano l'andamento e valutare l'impatto sulla qualità della vita. Possono essere descrittivi o analitici. Secondo la teoria epidemiologica, includono studi di coorte prospettici/retrospettivi, studi caso-controllo, studi solo su casi, studi trasversali, studi di appropriatezza e studi PASS - PAES.
- Studi Sperimentali: Progettati per rispondere alla domanda se una nuova procedura diagnostica o terapeutica funzioni e sia migliore rispetto alle pratiche correnti. Il modello di riferimento è lo studio clinico controllato randomizzato (RCT).
Lo Studio Clinico Controllato Randomizzato (RCT)
L'RCT è considerato il "gold standard" nella ricerca clinica, specialmente per la valutazione di trattamenti innovativi. La sua affidabilità deriva da caratteristiche fondamentali:
- Controllato: I partecipanti sono suddivisi in almeno due gruppi: uno riceve il trattamento sperimentale, l'altro (gruppo di controllo) riceve il trattamento standard o un placebo. Tutte le altre condizioni devono essere uniformi tra i gruppi per isolare l'effetto del trattamento.
- Randomizzato: L'assegnazione dei partecipanti ai gruppi di trattamento avviene in modo casuale. Questo processo elimina i bias di selezione e garantisce che i gruppi siano simili per tutti i fattori prognostici noti e ignoti, rendendo i risultati più attribuibili all'intervento studiato.
- Mascherato (Cieco): Per evitare influenze esterne, idealmente né il paziente né il ricercatore (e talvolta nemmeno chi analizza i dati) conoscono quale trattamento viene somministrato. Si parla di "cieco" (o "mascheramento" per ragioni di rispetto) singolo, doppio o triplo a seconda di chi è a conoscenza dell'assegnazione.
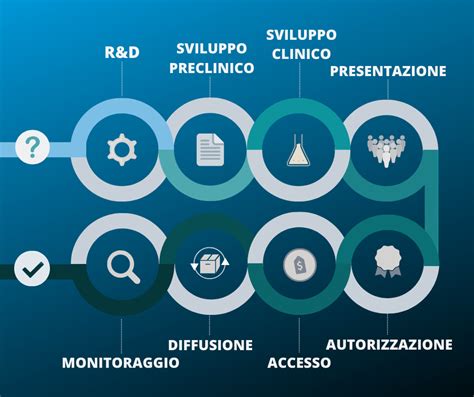
Le Fasi dello Sviluppo di un Farmaco: Un Percorso Rigoroso
Prima che un nuovo farmaco possa essere somministrato all'uomo, attraversa un lungo e rigoroso percorso di sperimentazione, suddiviso in diverse fasi:
Studi Preclinici: Condotti in laboratorio ("in vitro" su cellule o tessuti) e su animali ("in vivo"). Servono a conoscere le caratteristiche farmacologiche e tossicologiche della molecola, la sua stabilità chimica e a definire la formulazione e il dosaggio ottimale. Possono durare diversi anni.
Come si scopre un farmaco? Le fasi della #sperimentazione clinica e preclinica
Studi Clinici (sull'uomo): Se i risultati preclinici sono positivi, si procede alla sperimentazione sull'uomo, suddivisa in quattro fasi principali:
- Fase I: Valuta la sicurezza, la tollerabilità e la farmacocinetica del farmaco in un numero molto limitato di volontari (spesso sani, salvo eccezioni come i farmaci oncologici). L'obiettivo è identificare la massima dose tollerata e gli eventuali effetti indesiderati non emersi negli studi preclinici. Dura tipicamente 1-2 anni.
- Fase II: Indaga l'efficacia preliminare e gli effetti collaterali a breve termine del farmaco in un gruppo più ampio di pazienti (non più solo volontari sani). Si mira anche a stabilire la dose minima efficace. Circa il 33% dei farmaci supera questa fase.
- Fase III: Valuta comparativamente l'efficacia e la sicurezza del nuovo trattamento rispetto alle terapie standard o a un placebo, su larga scala, coinvolgendo centinaia o migliaia di pazienti in più centri di ricerca, anche internazionali. È la fase cruciale per confermare i benefici e il rapporto rischio/beneficio. Circa il 25% dei farmaci supera con successo questa fase, permettendo all'azienda di richiedere l'autorizzazione alla commercializzazione.
- Fase IV (Farmacovigilanza): Si svolge dopo l'immissione in commercio del farmaco. Monitora gli effetti indesiderati a lungo termine e rari che potrebbero manifestarsi in una popolazione più vasta e diversificata, raccogliendo dati sull'uso reale del farmaco nella pratica clinica quotidiana.
La Medicina Basata sulle Prove (Evidence-Based Medicine)
La medicina basata sulle prove (EBM) è un approccio che utilizza i risultati della ricerca clinica per informare le decisioni cliniche. Valuta la forza delle evidenze scientifiche, riconoscendo negli studi clinici controllati e randomizzati di buona qualità le prove più attendibili. Organizzazioni come la Cochrane Collaboration svolgono un ruolo fondamentale nel raccogliere e revisionare sistematicamente questi studi.
Tutela del Paziente e Consenso Informato
La partecipazione a uno studio clinico è un atto volontario e consapevole. Il paziente ha il diritto di ricevere informazioni complete e dettagliate prima di prendere una decisione. Questo processo avviene attraverso il Consenso Informato, un documento che descrive gli obiettivi dello studio, le procedure, i potenziali rischi e benefici, e i diritti del partecipante. È fondamentale che il paziente possa porre tutte le domande necessarie e che ogni dubbio venga chiarito. La presenza di un familiare o amico durante il colloquio con il medico può essere di grande aiuto.

Diritti e Garanzie per i Partecipanti
Oltre al consenso informato, la tutela dei partecipanti è garantita da diverse normative e linee guida internazionali e nazionali, tra cui:
- La Dichiarazione di Helsinki: Stabilisce i principi etici fondamentali per la ricerca medica che coinvolge esseri umani.
- Le Buone Pratiche Cliniche (GCP): Standard internazionali di etica e qualità scientifica per la progettazione, conduzione, registrazione e relazione degli studi clinici.
- Registri della ricerca clinica: Database pubblici che forniscono accesso alle informazioni sugli studi clinici in corso, promuovendo la trasparenza.
Il paziente è inoltre seguito da personale medico e paramedico esperto e competente per tutta la durata dello studio e anche nel periodo successivo (follow-up), e la sua privacy è rigorosamente tutelata.
L'Importanza della Ricerca Clinica e il Ruolo dei Cittadini
Nonostante la sua importanza cruciale, la ricerca clinica è ancora poco conosciuta e discussa nel nostro paese. L'emergenza pandemica ha evidenziato quanto la ricerca sia fondamentale per far fronte a sfide sanitarie globali. La partecipazione ai trial clinici rappresenta un'opportunità per accedere a terapie innovative e contribuire attivamente al progresso della medicina, migliorando la qualità della vita per i pazienti attuali e futuri. La scelta di partecipare è personale e va sempre discussa con il proprio medico di riferimento, ma la consapevolezza del processo e delle sue garanzie è un passo fondamentale per una decisione informata e responsabile.
tags: #studio #clinico #assistenziale

