Ammoniaca e Cervello: Un Legame Tossico nelle Malattie Oncologiche e Epatiche
L'interazione tra il sistema nervoso centrale e le disfunzioni metaboliche è un campo di studio complesso e di cruciale importanza, specialmente in contesti patologici avanzati come le malattie oncologiche e le epatopatie. Una delle sostanze che più chiaramente evidenzia questo legame è l'ammoniaca, un metabolita potenzialmente neurotossico la cui gestione errata da parte dell'organismo può avere ripercussioni devastanti sul cervello. Sebbene l'ammoniaca sia comunemente associata a patologie epatiche, recenti ricerche suggeriscono un suo coinvolgimento anche nella cachessia oncologica, una sindrome debilitante che affligge molti pazienti affetti da tumori in fase avanzata.
L'Ammoniaca: Un Metabolita da Gestire con Precisione
L'ammoniaca (NH3) è un sottoprodotto naturale del metabolismo delle proteine, generato principalmente dall'azione dei batteri intestinali e dal catabolismo muscolare. In un organismo sano, questa sostanza viene rapidamente neutralizzata e smaltita. La trasformazione principale avviene nel fegato, dove l'ammoniaca viene convertita in urea attraverso il ciclo dell'urea. L'urea è una molecola meno tossica che viene poi eliminata dall'organismo attraverso i reni con le urine. In condizioni fisiologiche, i livelli di ammoniaca nel sangue sono bassi, generalmente inferiori a 50 µmol/l.
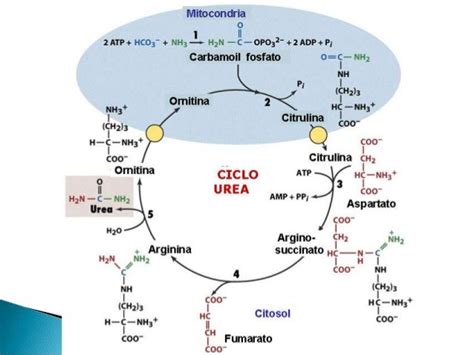
Tuttavia, quando il fegato è gravemente compromesso, come nel caso della cirrosi epatica, o in presenza di rari difetti enzimatici congeniti del ciclo dell'urea, questo meccanismo di smaltimento fallisce. Di conseguenza, l'ammoniaca si accumula nel flusso sanguigno, un fenomeno noto come iperammoniemia. Questa condizione non è una malattia in sé, ma piuttosto una manifestazione clinica di un disordine sottostante. L'ammoniaca accumulata può attraversare la barriera emato-encefalica, raggiungendo il cervello e esercitando un effetto tossico diretto sulle cellule cerebrali, in particolare sugli astrociti. Gli astrociti, cellule fondamentali per il supporto neuronale, utilizzano l'ammoniaca per sintetizzare la glutammina. Livelli elevati di glutammina nel cervello possono alterare l'equilibrio osmotico, portando al gonfiore degli astrociti e compromettendo la normale funzione cerebrale.
Encefalopatia Epatica: Il Cervello Sotto Attacco
L'accumulo di ammoniaca e altre tossine nel sangue, non più efficacemente filtrate dal fegato, è la causa principale dell'encefalopatia epatica (EH), nota anche come encefalopatia porto-sistemica. Questa condizione neurologica si manifesta con un'alterazione delle funzioni cerebrali, che può variare da lievi disturbi cognitivi a stati di coma profondo. L'EH è una complicazione comune e grave delle malattie epatiche avanzate, in particolare della cirrosi.
I sintomi dell'encefalopatia epatica si sviluppano solitamente in modo progressivo e vengono classificati in stadi di gravità, spesso utilizzando i criteri di West Haven:
- Grado 1 (Lieve): Caratterizzato da minima perdita della consapevolezza, euforia o ansia, diminuzione del grado di attenzione e difficoltà nei calcoli matematici semplici. Può manifestarsi con una lieve confusione mentale, irritabilità o un'inversione del ritmo sonno-veglia (insonnia notturna e sonnolenza diurna).
- Grado 2 (Moderato): Si osservano maggiori cambiamenti di personalità, letargia, stanchezza estrema e disorientamento spazio-temporale. Il paziente potrebbe non sapere dove si trova o che giorno sia.
- Grado 3 (Grave): Si manifestano linguaggio incoerente, sonnolenza marcata ma ancora risvegliabile, e in alcuni casi, convulsioni. Il paziente può entrare in uno stato di stupore, rispondendo solo a stimoli dolorosi.
- Grado 4 (Coma): Lo stadio più avanzato, in cui il paziente è in coma profondo e non responsivo agli stimoli.
Un segno patognomonico, particolarmente evidente negli stadi intermedi, è l'asterissi, un tremore involontario e brusco delle mani quando il paziente estende le braccia e piega i polsi all'indietro, simile a un battito d'ali. Altri sintomi neurologici possono includere disorientamento, amnesia, comportamento disinibito e peggioramento della capacità di scrittura manuale o di compiere piccoli movimenti con le mani. In alcuni casi, si può riscontrare un odore caratteristico dell'alito, definito "fetor hepaticus" o alito dolciastro/muffoso, causato dall'accumulo di sostanze solforate.
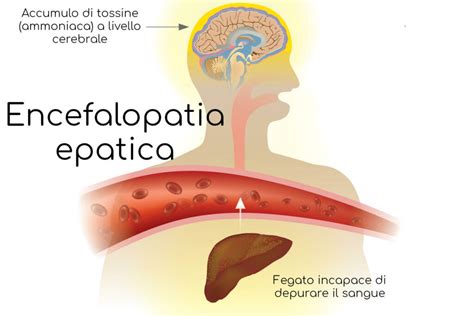
L'encefalopatia epatica può essere sia acuta, spesso legata a un'insufficienza epatica fulminante e potenzialmente trattabile con terapie d'emergenza o trapianto, sia cronica, innescata e sostenuta da un quadro di cirrosi epatica, con un'insorgenza più lenta e progressiva. Nei pazienti con cirrosi, il rischio di sviluppare EH è significativo, con circa il 20% di probabilità all'anno, e un'incidenza del 30-45% di EH conclamata in qualsiasi momento.
La Cachessia Oncologica: Oltre la Semplice Debolezza
Mentre l'encefalopatia epatica è strettamente legata a disfunzioni epatiche, una prospettiva più recente e intrigante riguarda il ruolo dell'ammoniaca e di meccanismi neuro-infiammatori nella cachessia oncologica. La cachessia colpisce circa l'80% dei pazienti affetti da tumori in fase avanzata, portando a un grave deperimento muscolare e a una perdita di peso nonostante un'alimentazione adeguata. Oncologi e caregiver conoscono molto bene i cambiamenti fisici ed emotivi che i pazienti oncologici spesso subiscono negli ultimi mesi di vita: sembrano svuotati di forza e di spirito. Anche chi ha mantenuto una visione positiva per tutta la vita può entrare in uno stato di disperazione.
Tradizionalmente, l'apatia, la mancanza di motivazione e il ritiro dalla vita sociale osservati nei pazienti oncologici terminali sono stati interpretati come una conseguenza psicologica inevitabile del deterioramento fisico. Tuttavia, una ricerca pubblicata su Science suggerisce che questi sintomi potrebbero non essere solo una reazione psicologica, ma veri e propri sintomi neurologici legati a una disfunzione specifica.
Adam Kepecs, del Department of Neuroscience della Washington University School of Medicine, spiega: "Abbiamo scoperto un circuito cerebrale completo che percepisce l'infiammazione nel flusso sanguigno e invia segnali che riducono la motivazione. Questo rivela che l'apatia non è solo una reazione emotiva o psicologica alla cachessia, ma è insita nella biologia della malattia". Questo circuito neuro-infiammatorio coinvolge tre regioni cerebrali chiave: l'area postrema (ArP), responsabile di nausea e vomito; il nucleo parabrachiale (PBN), che regola l'appetito; e la substantia nigra pars reticulata (SNpr), che può influenzare i livelli di dopamina.
La ricerca ha identificato l'interleuchina-6 (IL-6), una proteina rilasciata durante l'infiammazione e a lungo associata alla cachessia, come un segnale chiave. Nei topi di laboratorio con cachessia, la riduzione dei segnali dell'IL-6 nelle aree cerebrali collegate ha portato a un aumento della motivazione e a una minore sensibilità allo sforzo richiesto per ottenere cibo. Allo stesso modo, l'aumento dei livelli di dopamina in queste aree ha prodotto risultati simili.
Tobias Janowitz, professore associato del Cold Spring Harbor Laboratory (CSHL), sottolinea l'impatto di questi sintomi sulla vita dei pazienti: "Moltissimi pazienti oncologici lamentano sintomi di questa categoria. Dicono: 'Non so cosa mi stia succedendo. I miei parenti hanno cucinato il mio piatto preferito, ma non ho voglia di mangiarlo. I nipoti vengono a giocare con loro. Di solito sono entusiasti e si divertono, ora sembra che non si impegnino più di tanto'". La perdita di energia psicologica e motivazione non solo aggrava la sofferenza dei pazienti, ma li isola dalla famiglia e dagli amici. Poiché i pazienti faticano a impegnarsi in terapie pesanti che richiedono sforzo e perseveranza, ciò mette a dura prova anche le famiglie e complica il trattamento.
Mercoledì dell'Oncologia | Le neoplasie neuroendocrine: le linee guida AIOM
Implicazioni Terapeutiche e Nuove Prospettive
La comprensione del legame tra infiammazione, cachessia e alterazioni neurologiche apre nuove strade per il trattamento dei pazienti oncologici. La ricerca suggerisce che trattamenti anticorpali esistenti, mirati a bloccare l'azione di molecole infiammatorie come l'IL-6, potrebbero essere riproposti per migliorare la qualità di vita dei pazienti. "Il nostro obiettivo è far sentire meglio i pazienti e trattare meglio il cancro", spiega Janowitz. "Un paziente in uno stato più "fit" sarà in grado di tollerare meglio i trattamenti antitumorali e di trarne beneficio". La speranza è che, attraverso una continua collaborazione interdisciplinare, la cachessia possa essere trasformata in una condizione gestibile o superabile.
Per quanto riguarda l'encefalopatia epatica, il trattamento si concentra sulla riduzione della produzione di ammoniaca nell'intestino e sulla sua eliminazione. Il lattulosio, un lassativo non assorbibile, è il pilastro della terapia. Agisce acidificando il contenuto intestinale, convertendo l'ammoniaca in ione ammonio (NH4+), meno assorbibile, e accelerando il transito intestinale. Dosi di 15-30 ml vengono somministrate tre volte al giorno, e in caso di encefalopatia grave, possono essere utilizzati clisteri.
Antibiotici non assorbibili, come la rifaximina, sono un'altra opzione terapeutica importante. La rifaximina agisce riducendo selettivamente la popolazione di batteri intestinali produttori di ammoniaca, con un basso assorbimento sistemico e quindi minori effetti collaterali rispetto ad antibiotici in passato utilizzati come la neomicina.
Un approccio terapeutico innovativo che sta guadagnando terreno è il trapianto di flora batterica intestinale (trapianto fecale). Studi recenti indicano che questo intervento, in pazienti con encefalopatia epatica cronica e cirrosi, può migliorare significativamente le performance cognitive, aumentare la ricchezza della flora batterica intestinale con microrganismi benefici (come bifidobatteri e lattobacilli) e ridurre la probabilità di ricoveri ospedalieri correlati all'encefalopatia. Sebbene ancora in fase di valutazione su larga scala, il trapianto fecale dimostra il potenziale di manipolare attivamente il microbioma intestinale per influenzare la salute neurologica.

La gestione dell'encefalopatia epatica richiede anche un'attenzione particolare alla prevenzione di fattori scatenanti, come infezioni, emorragie gastrointestinali, squilibri elettrolitici e l'uso di alcuni farmaci psicotropi. In caso di insufficienza epatica acuta, il rischio di edema cerebrale massivo e morte è elevato, necessitando di interventi d'emergenza o, in casi critici, di un trapianto di fegato.
La Complessità della Tossicità Cerebrale
È importante sottolineare che, nonostante il ruolo centrale dell'ammoniaca, i livelli di ammoniemia nel sangue non sono sempre strettamente correlati alla gravità del danno cerebrale. Alcuni pazienti con livelli elevati possono non presentare alterazioni cerebrali evidenti, mentre altri con livelli più bassi possono mostrare sintomi significativi. Questo suggerisce che altri fattori, oltre all'ammoniaca stessa, contribuiscano alla neurotossicità nell'encefalopatia epatica. Anomalie nel sistema di neurotrasmissione GABA, squilibri tra amminoacidi aromatici e a catena ramificata, e la presenza di composti simili alle benzodiazepine sono state descritte e potrebbero giocare un ruolo.
Inoltre, la ricerca sull'encefalopatia etilmalonica ha messo in luce un altro meccanismo di tossicità cerebrale legato all'accumulo di sostanze tossiche. In questa rara malattia metabolica ereditaria, la carenza di una proteina mitocondriale (ETHE1) porta all'accumulo di acido solfidrico (H2S), un gas altamente tossico, nel cervello e in altri tessuti. Questo sottolinea come diverse vie metaboliche e accumuli di metaboliti tossici possano compromettere gravemente la funzione cerebrale, anche in assenza di disfunzioni epatiche primarie.
La determinazione dell'ammoniemia rimane uno strumento diagnostico fondamentale, utilizzato principalmente per supportare la diagnosi di gravi patologie epatiche e per indagare le cause di alterazioni dello stato di coscienza, specialmente in casi di coma di origine sconosciuta o per supportare la diagnosi di sindrome di Reye o encefalopatia epatica. Può essere richiesta anche per valutare la gravità di disordini del metabolismo che coinvolgono il ciclo dell'urea.
La correlazione tra il consumo di alcol e un aumentato rischio di tumori del colon-retto, confermata da ricerche epidemiologiche, evidenzia ulteriormente l'impatto di sostanze tossiche sull'organismo e la loro potenziale interconnessione con diverse patologie. Allo stesso modo, l'aumento delle vendite di bevande analcoliche o a basso contenuto alcolico ("NoLo") riflette una crescente consapevolezza dei rischi associati al consumo di alcol e la ricerca di alternative percepite come più salutari, un tema di salute pubblica di crescente rilevanza.
In conclusione, la relazione tra ammoniaca, cervello e malattie oncologiche ed epatiche è un campo di ricerca in rapida evoluzione. Mentre l'encefalopatia epatica rimane una complicanza ben studiata legata all'accumulo di ammoniaca dovuta a disfunzioni epatiche, la scoperta di circuiti neuro-infiammatori che influenzano la motivazione e il comportamento nei pazienti oncologici affetti da cachessia apre nuove prospettive diagnostiche e terapeutiche. La comprensione profonda di questi meccanismi è essenziale per migliorare la qualità di vita e le opzioni di trattamento per i pazienti affetti da patologie gravi e complesse.
tags: #malati #oncologici #ammoniaca #cervello

