La Cellula Tumorale: Un'Egoista Ribelle alla Cooperazione Biologica
Ogni cellula all'interno di un organismo pluricellulare porta in sé il potenziale latente di trasformarsi in una cellula tumorale. Questa predisposizione affonda le sue radici in un retaggio evolutivo ancestrale, quando le cellule vivevano in un'era di autonomia, occupandosi esclusivamente del proprio sostentamento e della propria riproduzione, senza la necessità di cooperare con altre entità per la sopravvivenza dell'organismo. La pluricellularità ha portato allo sviluppo di sofisticati meccanismi di controllo, progettati per identificare ed eliminare le cellule che manifestano un ritorno a comportamenti "egoistici", deviando dalle norme cooperative. Tuttavia, come ogni sistema, anche quelli biologici più complessi non sono immuni da errori, e una piccola percentuale di deviazioni è inevitabile.
Il Paradosso di Peto e la Resistenza degli Elefanti
L'aumento del numero di cellule in un organismo si traduce intrinsecamente in un incremento del rischio che una di esse possa subire trasformazioni maligne. Questo principio è osservabile all'interno della stessa specie, dove l'incidenza dei tumori tende ad aumentare proporzionalmente alla crescita dimensionale degli individui. Sorprendentemente, questo trend non si mantiene quando si confrontano specie diverse, un fenomeno noto come il "paradosso di Peto". Tra le specie che più alimentano questo paradosso spiccano gli elefanti. Nonostante le loro dimensioni colossali, gli elefanti presentano una probabilità di sviluppare malattie tumorali paragonabile a quella di un piccolo topo.

Un'indagine condotta da ricercatori delle università della California e di Buffalo ha mirato a svelare i meccanismi dietro questa straordinaria resistenza ai tumori nei pachidermi. L'attenzione si è concentrata sugli Afroteri, un superordine di mammiferi che annovera organismi di taglia estremamente variabile, dalle talpe dorate di appena 70 grammi agli elefanti africani che possono superare le 6 tonnellate. In questo gruppo, il gigantismo è un tratto evolutivo che si è manifestato indipendentemente in almeno tre occasioni: nelle procavie, nelle mucche di mare e, naturalmente, negli elefanti.
I ricercatori hanno ricostruito la storia evolutiva degli Afroteri, analizzando l'evoluzione della massa corporea e del rischio oncologico, prestando particolare attenzione alle variazioni dei geni noti per il loro ruolo di soppressori tumorali, come TP53 e LIF. La scoperta più sorprendente è stata la presenza comune di duplicazioni nei geni deputati alla riduzione del rischio tumorale in tutti gli Afroteri, indipendentemente dalla loro taglia. Negli elefanti, tuttavia, queste duplicazioni sembrano partecipare a processi unici che potrebbero spiegare la loro eccezionale resilienza. L'aumento delle dimensioni corporee e l'evoluzione dei meccanismi antitumorali negli Afroteri si sono verificati per gradi: da organismi di piccole dimensioni a quelli di taglia media, poi a quelli grandi, fino a raggiungere dimensioni gigantesche, come nel caso del Palaeoloxodon antiquus, un estinto elefante dalle zanne dritte che poteva pesare tra le 10 e le 13 tonnellate.
Ulteriori ricerche hanno rivelato che, sia nei sirenidi che nei proboscidati, le duplicazioni del gene TP53, un fondamentale soppressore tumorale, sono state precedute da duplicazioni nei geni GTF2F1, STK11 e BRD7 negli antenati Afroteri di dimensioni minori. Questi tre geni sono cruciali nella regolazione della trascrizione di TP53. Pertanto, la loro duplicazione precoce ha fornito una base fondamentale per la piena funzionalità di TP53, consentendo agli animali di aumentare significativamente le proprie dimensioni senza incorrere in un rischio oncologico proporzionalmente maggiore. Le cellule degli elefanti, in particolare, dimostrano una notevole resistenza allo stress ossidativo, una capacità di riparazione del DNA eccezionalmente rapida e una resistenza all'immortalizzazione, una caratteristica tipica delle cellule tumorali, anche in condizioni di laboratorio.
La Complessa Danza Molecolare del Cancro
Il cancro, nella sua essenza, nasce da cellule sane che, a seguito di mutazioni nel DNA, subiscono alterazioni profonde nei loro normali processi biologici. Milioni di persone affette da tumore nel mondo condividono una comune anomalia genetica: mutazioni nel gene che codifica per la proteina p53, uno dei più potenti soppressori tumorali. In molti casi, queste mutazioni non inattivano la proteina p53, ma la modificano, trasformandola in un attore chiave nella progressione maligna.
Il ruolo di p53 nel cancro
La ricerca condotta dal gruppo di Giannino Del Sal, professore di Biologia Applicata all'Università di Trieste, ha portato alla luce un aspetto cruciale e precedentemente sconosciuto di p53 e del cancro. Si è scoperto che particolari condizioni fisiche del tessuto tumorale, come la sua durezza, rigidità e la forte tensione interna, spesso presenti nei tumori più aggressivi, possono stabilizzare e stimolare l'attività della p53 mutata. Le cellule tumorali, in risposta a queste anomalie meccaniche, attivano una cascata di segnali biochimici che potenziano la p53 mutata, inibendo i meccanismi cellulari deputati alla sua degradazione. In sostanza, l'organizzazione strutturale del tessuto tumorale diventa più rigida, e questa rigidità, a sua volta, favorisce la proliferazione della cellula malata.
La ricerca scientifica, fino a questo punto, si era concentrata principalmente sui segnali chimici che guidano i comportamenti aggressivi del tumore. Tuttavia, il lavoro di Del Sal e collaboratori ha stabilito un legame diretto tra le anomalie meccaniche dei tessuti malati e l'alterazione genetica più frequente nei tumori, ovvero quella che porta alla produzione di una proteina p53 mutata. La proteina p53 mutata, infatti, innesca un circuito di auto-rinforzo, alimentato dalla riprogrammazione del metabolismo cellulare del colesterolo. La via di sintesi del colesterolo è la stessa che la p53 mutata è in grado di attivare, e alcuni suoi prodotti intermedi si rivelano fondamentali per la stabilità della proteina mutata e per la capacità della cellula tumorale di adattarsi alle condizioni ambientali.
Questo scenario complesso è stato delineato attraverso un'integrazione di diverse analisi, che hanno spaziato dallo studio delle vie molecolari cellulari all'analisi dello stato fisico dei tessuti tumorali, includendo la misurazione dell'espressione genica, della rigidità e della composizione cellulare e del suo microambiente. La ricerca ha anche esplorato centinaia di composti chimici per identificare nuove molecole in grado di eliminare la p53 mutata dalle cellule tumorali, con un'attenzione particolare alle statine, farmaci comunemente usati per l'ipercolesterolemia. Questo ha portato a concentrarsi sulla via di sintesi del colesterolo, rivelando un legame precedentemente sconosciuto tra le alterazioni metaboliche in questa via, la rigidità tumorale e la stabilità della p53 mutata.
È noto da tempo che i tumori presentano ritmi metabolici accelerati rispetto ai tessuti normali, un vantaggio cruciale per la loro sopravvivenza. La scoperta del legame tra le alterazioni metaboliche nella via del colesterolo e la rigidità tumorale apre nuove prospettive terapeutiche. I ricercatori hanno dimostrato, in cellule isolate e animali da laboratorio, che intervenendo su questo aspetto del metabolismo tumorale è possibile destabilizzare la p53 mutata, ripristinare le proprietà meccaniche del tessuto e arrestare la progressione tumorale. Questo traguardo chiude un importante programma di ricerca in Oncologia Molecolare Clinica, focalizzato su uno dei sottotipi più aggressivi di tumore al seno, i tumori triplo-negativi.
Autonomia Cellulare e Riserva Funzionale: Oltre la Genetica
Quando si discute di tumore del polmone, l'attenzione si concentra spesso su stadio, istologia, alterazioni molecolari e opzioni terapeutiche. Sebbene questi fattori siano decisivi, due pazienti con la stessa diagnosi e lo stesso trattamento possono avere percorsi clinici radicalmente diversi, con recuperi post-operatori, tolleranza alle terapie e livelli di qualità della vita che divergono significativamente. La qualità della vita (QOL) è un'esperienza vissuta, influenzata dallo stress sistemico del tumore e dallo stress aggiuntivo imposto dalle terapie oncologiche.
La diminuzione del VO₂peak, il picco di consumo di ossigeno, non è solo un dato fisiologico, ma un indicatore della capacità dell'organismo di trasportare e utilizzare ossigeno, misurando la "potenza del motore" del corpo. Il muscolo scheletrico, lungi dall'essere un mero tessuto meccanico, è un organo endocrino attivo che produce miochine con effetti immunomodulatori e anti-infiammatori. L'esercizio fisico, ad esempio, può aumentare l'infiltrazione di cellule natural killer (NK) nel tumore e modulare l'ambiente immunitario.
Il performance status (PS) rimane uno strumento utile, ma presenta limiti evidenti. Studi sulla composizione corporea nei pazienti con carcinoma polmonare non a piccole cellule (NSCLC) resecabile hanno evidenziato una frequente perdita di massa muscolare, anche negli stadi iniziali, con impatti sul recupero post-operatorio e sulla tolleranza ai trattamenti. Sempre più evidenze suggeriscono che la funzione fisica e la QOL non siano solo conseguenze della malattia, ma possano predire gli esiti clinici a lungo termine.
Nel carcinoma polmonare in stadio iniziale, la chirurgia rappresenta la terapia principale e potenzialmente curativa. Uno studio prospettico su pazienti anziani sottoposti a resezione polmonare per NSCLC ha mostrato un calo prevedibile della QOL nel periodo post-operatorio, con un recupero verso i valori basali entro tre mesi. Fattore chiave associato a questo recupero è la capacità di mantenere la distanza percorsa nel test del cammino di 6 minuti (6MWT) nel periodo perioperatorio.
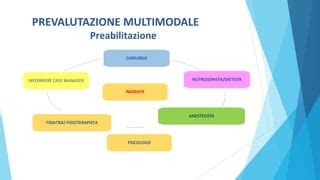
Qui entra in gioco la "preabilitazione", un percorso multidisciplinare pre-operatorio (o pre-trattamento) volto a ottimizzare le condizioni fisiche, nutrizionali e psicologiche del paziente. Una revisione della letteratura sui programmi di esercizio preoperatorio nei pazienti con NSCLC ha indicato che l'allenamento prima dell'intervento è associato a una significativa riduzione del rischio di complicanze polmonari post-operatorie, a una diminuzione della degenza ospedaliera e a un miglioramento della performance nel 6MWT. La preabilitazione non si limita a "allenare" il paziente, ma mira al mantenimento delle sue capacità funzionali.
Nei pazienti trattati con terapie target, la sopravvivenza si è allungata, trasformando la malattia in una condizione cronica. In questo contesto, la valutazione della sola risposta radiologica non è più sufficiente; diventano centrali la stabilità dei sintomi, il mantenimento dell'autonomia e la preservazione della capacità funzionale nel tempo. Studi recenti hanno dimostrato che, anche con un controllo della malattia, la fatica e il declino dell'attività fisica possono incidere significativamente sulla QOL percepita.
Le Caratteristiche Distintive della Cellula Neoplastica
Indipendentemente dal tessuto di origine, le cellule tumorali condividono una serie di caratteristiche distintive che le differenziano dalle cellule normali. Queste includono:
- Autosufficienza nei segnali di crescita: Le cellule tumorali non dipendono da segnali esterni per proliferare. Proteine come quelle della famiglia Ras e Myc giocano un ruolo chiave nell'attivazione di vie di trasduzione del segnale che promuovono la crescita cellulare.
- Inibizione dei processi apoptotici: Le cellule tumorali evitano la morte cellulare programmata (apoptosi), un meccanismo fondamentale per l'eliminazione delle cellule danneggiate o superflue. Il gene TP53, un soppressore tumorale chiave, è spesso mutato in questo contesto.
- Insensibilità ai segnali anti-proliferativi: Segnali che normalmente inibiscono la crescita cellulare vengono ignorati dalle cellule tumorali. La proteina retinoblastoma (pRb), un altro importante soppressore tumorale, è spesso inattivata.
- Potenziale replicativo illimitato: A differenza delle cellule sane, che hanno un numero definito di divisioni possibili (legate all'accorciamento dei telomeri), le cellule tumorali acquisiscono la capacità di replicarsi indefinitamente.
- Capacità di stimolare l'angiogenesi: Per soddisfare le loro crescenti esigenze metaboliche, le cellule tumorali promuovono la formazione di nuovi vasi sanguigni attraverso la produzione di fattori come il VEGF (Vascular Endothelial Growth Factor).
- Capacità di invadere e metastatizzare: Le cellule tumorali possono staccarsi dal tumore primario, invadere i tessuti circostanti e diffondersi ad altre parti del corpo attraverso i vasi sanguigni e linfatici, formando metastasi.

Queste caratteristiche intrinseche della cellula tumorale sono spesso accompagnate da profonde alterazioni nelle sue interazioni con il microambiente tumorale. Le cellule tumorali possono "educare" le cellule circostanti, inclusi quelle immunitarie e stromali, a sostenere la loro crescita invasiva e la formazione di metastasi.
Deregolazione Metabolica: L'Effetto Warburg e Oltre
Un'altra caratteristica fondamentale delle cellule tumorali è la deregolazione del metabolismo. Questo comportamento complesso e spesso specifico dei diversi sottotipi tumorali consente loro di adattarsi alle condizioni di crescita e sopravvivenza. Uno dei primi meccanismi metabolici messi in atto è un efficace approvvigionamento di nutrienti, ottenuto tramite l'aumento dell'espressione dei trasportatori di glucosio e aminoacidi. Questo fenomeno è noto come "effetto Warburg", dove le cellule tumorali preferiscono la glicolisi, anche in presenza di ossigeno, per produrre energia.
Sebbene la respirazione cellulare sia più efficiente in termini di produzione di ATP, la glicolisi accelerata nelle cellule tumorali offre diversi vantaggi. Fornisce intermedi metabolici necessari per la sintesi di nuove molecole (aminoacidi, proteine, lipidi), essenziali per la costruzione di nuove cellule e l'aumento della biomassa tumorale. Inoltre, la glicolisi genera un ambiente acido che può favorire l'invasione tissutale.
Oltre al glucosio, i tumori si nutrono in modo amplificato anche di aminoacidi come la glutammina, fondamentale per la sintesi di basi azotate e quindi di acidi nucleici. I cambiamenti metabolici influenzano anche le cellule stromali e immunitarie che infiltrano il tessuto tumorale. Le cellule tumorali, secernendo fattori solubili, "educano" le cellule circostanti a riconvertire il loro metabolismo in modo opportunistico, creando relazioni a senso unico.
Le ricerche in questo campo hanno aperto nuove prospettive terapeutiche, mirando a sfruttare le specifiche vulnerabilità metaboliche delle cellule tumorali. Ad esempio, strategie che bloccano la glicolisi o la sintesi di aminoacidi potrebbero rappresentare approcci terapeutici efficaci.
L'Orologio Biologico e la Vulnerabilità Tumorale
Una prospettiva innovativa nella lotta contro il cancro emerge dalla ricerca sull'orologio biologico delle cellule. Le nostre cellule possiedono meccanismi molecolari che regolano le loro attività nelle 24 ore, seguendo il ritmo circadiano. Alterazioni di questo ritmo sono state associate a un aumento del rischio di cancro.
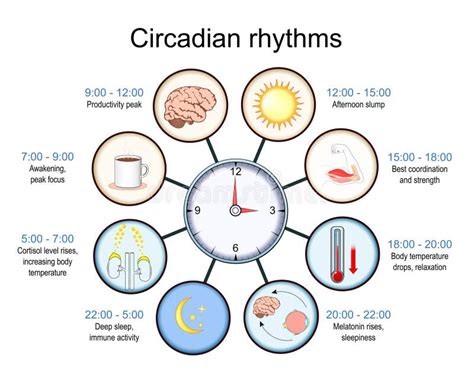
Studi condotti in California hanno dimostrato che l'attivazione farmacologica delle proteine REV-ERB, coinvolte nel controllo del ritmo circadiano, può essere letale per le cellule tumorali, risparmiando quelle sane. Questo approccio agisce bloccando simultaneamente diversi meccanismi cellulari che le cellule tumorali utilizzano per procurarsi il nutrimento necessario alla loro rapida crescita, come l'autofagia (il riciclo di componenti cellulari) e la sintesi dei grassi. A differenza dei farmaci tradizionali che colpiscono un singolo bersaglio, l'azione sull'orologio biologico sfrutta molteplici vulnerabilità delle cellule tumorali.
Autofagia e Mitosi: Bersagli Molecolari
Un'altra linea di ricerca promettente riguarda il blocco dei meccanismi di riciclo delle proteine e di riproduzione delle cellule tumorali. L'autofagia, un processo di riciclo cellulare, può svolgere un duplice ruolo nei tumori, favorendo la sopravvivenza o la morte cellulare a seconda del contesto. Una molecola identificata da ricercatori del CNR-IBPM è in grado di bloccare una fase specifica dell'autofagia e, contemporaneamente, la mitosi, il processo attraverso il quale una cellula si divide in due cellule figlie.
Questa molecola agisce bloccando le fasi tardive dell'autofagia, impedendo la fusione tra il materiale da degradare e i lisosomi, gli organelli deputati alla demolizione delle proteine. L'attività di questa molecola impedisce la degradazione e il riciclo di materiali cellulari deteriorati, rendendoli tossici per la cellula. Nei tipi di tumore che dipendono da un'autofagia funzionale per la sopravvivenza, come il glioblastoma e gli adenocarcinomi duttali pancreatici, questa molecola potrebbe rivelarsi un efficace inibitore.
La Cellula Tumorale come Organismo Indipendente
Fondamentalmente, una cellula tumorale si distingue per la sua indipendenza dai parametri di condivisione dell'ambiente e del tessuto in cui origina. Questa autonomia porta a uno squilibrio delle normali funzioni fisiologiche e, di conseguenza, alla malattia. Le cellule tumorali mostrano alterazioni nel controllo genetico della divisione cellulare e sviluppano relazioni complesse con il loro microambiente.
Il Ruolo dello Stress Ossidativo e del Metabolismo Energetico
Le cellule tumorali presentano spesso una maggiore resistenza ai danni dello stress ossidativo e possono proteggersi da esso, favorendo la loro sopravvivenza e diffusione. La loro sopravvivenza, tuttavia, dipende dall'ossigeno molecolare, che funge da segnale e processo di trasporto.
La preferenza per la fermentazione lattica, anche in presenza di ossigeno (effetto Warburg), suggerisce un adattamento metabolico specifico delle cellule tumorali. Questo processo, sebbene meno efficiente in termini di produzione di energia rispetto alla fosforilazione ossidativa mitocondriale, fornisce intermedi metabolici cruciali per la biosintesi e può contribuire alla resistenza all'apoptosi. La deregolazione di trasportatori del glucosio e di enzimi come la piruvato deidrogenasi chinasi (PDK) gioca un ruolo chiave nel reindirizzare il piruvato verso la fermentazione anziché verso il ciclo dell'acido citrico.
Apoptosi e Resilienza Cellulare
L'apoptosi, o morte cellulare programmata, è un processo fondamentale per il mantenimento dell'omeostasi tissutale. Le cellule tumorali, evadendo l'apoptosi, acquisiscono un vantaggio proliferativo. L'attivazione dell'apoptosi può essere indotta da vari fattori, tra cui il danno al DNA e lo stress ossidativo.
La via apoptotica mitocondriale, che coinvolge il rilascio di citocromo C nello spazio intermembrana mitocondriale, è un meccanismo chiave. L'attivazione di caspasi, una famiglia di proteasi, porta alla degradazione dei componenti cellulari e alla morte della cellula. La comprensione dei meccanismi che regolano l'apoptosi è fondamentale per lo sviluppo di terapie antitumorali mirate.
Nuove Frontiere Terapeutiche
La ricerca continua a esplorare nuove strategie terapeutiche per combattere il cancro. L'identificazione di molecole in grado di riattivare proteine soppressorie tumorali, di interferire con il metabolismo cellulare o di ripristinare i ritmi circadiani delle cellule apre scenari promettenti. La comprensione approfondita delle caratteristiche intrinseche della cellula tumorale e delle sue interazioni con l'ambiente circostante è la chiave per sviluppare approcci terapeutici più efficaci e meno tossici.
La Complessità dell'Origine del Cancro
L'origine del cancro è un fenomeno multifattoriale, che coinvolge un complesso intreccio di fattori genetici, epigenetici e ambientali. Non si tratta di un evento singolo, ma di un processo a tappe che porta a una progressione della malattia. Le alterazioni nella regolazione dei geni, le mutazioni selettive e le modifiche epigenetiche creano il terreno ideale per l'insorgenza e la progressione neoplastica.
La capacità delle cellule tumorali di eludere i meccanismi di controllo dell'organismo, come le cellule NK del sangue, contribuisce alla loro sopravvivenza e diffusione. Comprendere la "musica della vita", come la definisce il fisiologo Denis Noble, ovvero l'interazione dinamica tra geni, proteine e ambiente, è essenziale per decifrare la complessità del cancro.
La ricerca si muove verso un approccio integrato, che considera la cellula tumorale non solo come un'entità isolata, ma come parte di un sistema complesso, in cui le interazioni con l'ambiente circostante, il metabolismo energetico e i meccanismi di regolazione genica giocano ruoli cruciali. Questo approccio olistico è fondamentale per sviluppare terapie realmente efficaci nel contrastare questa complessa malattia.
tags: #autosufficienza #cellula #tumorale

