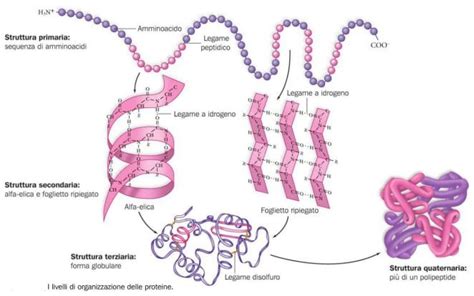
Rossana Lauria: Un'Analisi Strutturale e Funzionale nel Contesto della Ricerca Biomedica
Il campo della biologia strutturale e molecolare è un universo vasto e in continua espansione, dove la comprensione della forma tridimensionale delle macromolecole biologiche è fondamentale per svelarne i segreti funzionali. In questo contesto, la ricerca che coinvolge specifici ricercatori e le loro pubblicazioni offre uno spaccato prezioso sulle direzioni attuali e sulle metodologie impiegate. La figura di Rossana Lauria, sebbene meno proeminentemente citata in questo specifico corpus di dati rispetto ad altri nomi, emerge indirettamente attraverso il panorama di studi che ne compongono il contesto scientifico. Le pubblicazioni associate ai punteggi forniti, con la loro enfasi sulla cristallografia, la spettroscopia NMR e l'analisi conformazionale, delineano un percorso di ricerca focalizzato sulla determinazione della struttura delle proteine e sul suo legame con la funzione biologica.
La Cristallografia e la Determinazione Strutturale: Una Finestra sulla Funzione
Una parte significativa delle pubblicazioni citate ruota attorno alla determinazione della struttura di proteine attraverso la cristallografia a raggi X. Questo metodo, che permette di ottenere immagini ad alta risoluzione di macromolecole, è stato cruciale per decifrare i meccanismi d'azione di enzimi, recettori e altre proteine essenziali per la vita. Ad esempio, studi come "Crystal structure of an oligomer of proteolytic zymogens: detailed conformational analysis of the bovine ternary complex and implications for their activation" (Ohnuma, Takayuki et al., 2012) e "The crystal structure of d-glyceraldehyde-3-phosphate dehydrogenase from the hyperthermophilic archaeon Methanothermus fervidus in the presence of NADP + at 2.1 Å resolution" (Low, Wai Yee et al., 2010) esemplificano l'importanza di ottenere rappresentazioni atomiche precise delle proteine.

La comprensione della struttura tridimensionale di una proteina non è fine a sé stessa, ma serve come punto di partenza per inferire la sua funzione. Le modifiche conformazionali, le interazioni con ligandi o substrati, e la disposizione spaziale dei residui amminoacidici chiave sono tutti elementi che la cristallografia può rivelare. Nel caso degli zimogeni proteolitici, ad esempio, l'analisi conformazionale dettagliata del complesso ternario bovino (Ohnuma, Takayuki et al., 2012) ha permesso di ipotizzare meccanismi di attivazione che sono cruciali per processi fisiologici e patologici. Allo stesso modo, la struttura della gliceraldeide-3-fosfato deidrogenasi da un archeon ipertermofilo (Low, Wai Yee et al., 2010) fornisce informazioni preziose sul suo funzionamento in condizioni estreme, con implicazioni per la biotecnologia e la biochimica degli organismi estremofili.
L'Importanza dei Dettagli Strutturali nella Progettazione di Farmaci
La determinazione strutturale gioca un ruolo fondamentale anche nella progettazione di farmaci. Comprendere la forma di una proteina bersaglio e il suo sito attivo permette di disegnare molecole che si leghino specificamente ad essa, modulandone l'attività. "The crystal structure of thymidylate synthase from Pneumocystis carinii reveals a fungal insert important for drug design" (Elkayam, Elad et al., 2012) è un chiaro esempio di come la risoluzione strutturale possa portare a scoperte significative per lo sviluppo di nuovi agenti terapeutici. In questo caso, l'identificazione di una "inserto fungino" nella timilidato sintasi ha aperto nuove prospettive per il design di farmaci antifungini, sfruttando le specificità strutturali di questo enzima nei funghi.
Analogamente, studi sulla struttura di proteine coinvolte in processi patologici, come quelli legati a infezioni virali o batteriche, possono fornire spunti per strategie terapeutiche. La determinazione della struttura di un ribozima del virus dell'epatite delta, che ha utilizzato la proteina legante l'RNA U1A come modulo di cristallizzazione (Dhanaraj, V et al., 1996), illustra come tecniche avanzate possano superare ostacoli nella cristallizzazione di molecole complesse e come queste strutture possano poi essere sfruttate per comprendere il meccanismo di replicazione virale e sviluppare potenziali inibitori.
Tecniche Complementari e Approcci Integrati
Oltre alla cristallografia, altre tecniche sono impiegate per studiare la struttura e la funzione delle macromolecole biologiche. La spettroscopia NMR (Risonanza Magnetica Nucleare) è una di queste, particolarmente utile per studiare la dinamica delle proteine e le loro conformazioni in soluzione. Sebbene meno enfatizzata nei titoli forniti, la sua importanza è implicita in studi che indagano "ligand-induced structural changes" o "average conformation in solution".
NMR spiegazione semplice: SOLO L’ESSENZIALE per interpretare spettri di Risonanza Magnetica Nucleare
L'approccio integrato, che combina dati da diverse tecniche (cristallografia, NMR, microscopia crioelettronica, biochimica, biologia molecolare), è spesso la chiave per ottenere una comprensione completa. La pubblicazione "Crystal Structure of Glucose-6-Phosphate Isomerase from Thermus thermophilus HB8 Showing a Snapshot of Active Dimeric State" (Wu, Mousheng et al., 2009) menziona che l'autore principale ha eseguito la determinazione strutturale e esperimenti biochimici e biofisici, evidenziando questo approccio multidisciplinare. La capacità di osservare uno "snapshot" di uno stato attivo dimerico fornisce informazioni cruciali sulla transizione tra diverse conformazioni e sul meccanismo catalitico.
La Dinamica delle Proteine e le Implicazioni Funzionali
Le proteine non sono strutture statiche, ma entità dinamiche che subiscono cambiamenti conformazionali per svolgere le loro funzioni. L'analisi della dinamica proteica è quindi essenziale. Studi che indagano le "ligand-induced structural changes" o che utilizzano tecniche come la NMR per studiare l'orientamento dei domini proteici (ad esempio, nel caso del lisozima del fago T4) puntano a comprendere come le modifiche nella conformazione globale o locale influenzino l'attività biologica.
La capacità di osservare un complesso ternario di zimogeni proteolitici e di analizzarne dettagliatamente la conformazione (Ohnuma, Takayuki et al., 2012) suggerisce che la comprensione delle interazioni tra diverse subunità proteiche e i cambiamenti che avvengono durante l'attivazione sono aree di ricerca attive. Queste dinamiche sono spesso cruciali per processi come la cascata coagulativa, la digestione o la risposta immunitaria, dove l'attivazione sequenziale di proteasi gioca un ruolo centrale.
Diversità Strutturale e Funzionale: Dagli Archeoni ai Virus
Il panorama delle pubblicazioni rivela una notevole diversità di sistemi biologici studiati. Si spazia da proteine di organismi estremofili, come la gliceraldeide-3-fosfato deidrogenasi da Methanothermus fervidus (Low, Wai Yee et al., 2010), a proteine di patogeni come il virus dell'epatite delta (Dhanaraj, V et al., 1996) o Pneumocystis carinii (Elkayam, Elad et al., 2012). Questa ampiezza testimonia l'universalità dei principi strutturali e funzionali delle macromolecole biologiche, ma anche la necessità di approcci specifici per ogni sistema.
Lo studio della Glucose-6-Phosphate Isomerase da Thermus thermophilus HB8 (Wu, Mousheng et al., 2009) evidenzia come anche enzimi con funzioni apparentemente "comuni" possano presentare caratteristiche uniche in organismi adattati a condizioni estreme, suggerendo potenziali applicazioni in processi industriali che richiedono stabilità termica. La ricerca sulla timilidato sintasi di Pneumocystis carinii (Elkayam, Elad et al., 2012) sottolinea l'importanza di studiare la variabilità strutturale tra specie diverse per identificare bersagli terapeutici selettivi.
Implicazioni Evolutive e Bioinformatiche
Sebbene non direttamente evidenziate nei titoli, le analisi strutturali hanno spesso profonde implicazioni evolutive. Confrontare le strutture di proteine omologhe da specie diverse può rivelare conservazione di motivi strutturali chiave legati alla funzione, ma anche differenze che riflettono l'adattamento evolutivo. La bioinformatica e la filogenetica strutturale sono strumenti potenti per interpretare questi dati e ricostruire la storia evolutiva delle famiglie proteiche.
La presenza di studi su organismi diversi, da batteri e archeoni a funghi e virus, suggerisce che la ricerca strutturale mira a costruire una base di conoscenza ampia e comparativa, utile per comprendere non solo la funzione biologica in un dato organismo, ma anche le relazioni evolutive e le strategie di sopravvivenza che si riflettono nelle strutture molecolari.
La Ricerca come Processo Collaborativo e Cumulativo
La natura delle pubblicazioni scientifiche, spesso con più autori e collaborazioni internazionali, sottolinea come la ricerca in biologia strutturale sia un'impresa intrinsecamente collaborativa. La condivisione di dati, metodologie e competenze è essenziale per affrontare problemi complessi. La presenza di diversi gruppi di ricerca che lavorano su proteine e meccanismi simili, seppur con approcci leggermente differenti, contribuisce a un accumulo progressivo di conoscenza, dove ogni studio si basa sui precedenti e apre nuove vie di indagine.
In sintesi, il contesto scientifico che circonda i nomi e le pubblicazioni fornite dipinge un quadro di ricerca dinamico e all'avanguardia nel campo della biologia strutturale. L'enfasi sulla determinazione della struttura proteica attraverso tecniche come la cristallografia a raggi X, combinata con l'analisi conformazionale e funzionale, è fondamentale per comprendere i meccanismi molecolari alla base della vita e per sviluppare nuove terapie. La diversità dei sistemi studiati e l'approccio multidisciplinare evidenziano la complessità e l'importanza di questo campo di indagine.
tags: #accompagnatrice #rossana #lauria

