Anemia nel Malato Oncologico: Cause, Sintomi e Strategie Terapeutiche
L'anemia nei pazienti affetti da neoplasie è una condizione clinica complessa, che va ben oltre la semplice carenza nutrizionale. Si tratta di una sindrome multifattoriale, caratterizzata da una riduzione dei livelli di emoglobina, dei globuli rossi o dell'ematocrito, che scaturisce dall'interazione patologica tra le cellule tumorali e il sistema immunitario dell'ospite. La presenza di un tumore innesca una risposta infiammatoria cronica, che altera profondamente la produzione e la sopravvivenza dei globuli rossi, rendendo questa condizione una forma di anemia da malattia cronica (o anemia da infiammazione) con specificità oncologiche.
Nel contesto oncologico, a questo meccanismo si sovrappongono frequentemente altri fattori scatenanti, quali perdite ematiche croniche, l'infiltrazione del midollo osseo da parte delle cellule neoplastiche, e gli effetti tossici intrinseci dei farmaci antiblastici e della radioterapia. La comprensione di queste cause è fondamentale per un approccio diagnostico e terapeutico efficace.
Le Molteplici Cause dell'Anemia Oncologica
Le ragioni per cui un paziente oncologico sviluppa anemia sono numerose e spesso coesistono nello stesso individuo, contribuendo a un quadro clinico complesso.
Infiammazione Cronica e Citochine: Il Meccanismo Primario
Il tumore agisce come un potente stimolo per il sistema immunitario, inducendo la produzione di citochine pro-infiammatorie, tra cui spiccano l'interleuchina-6 (IL-6), il fattore di necrosi tumorale alfa (TNF-alfa) e l'interferone-gamma (IFN-gamma). Queste molecole messaggere svolgono un ruolo cruciale nella patogenesi dell'anemia. In particolare, l'IL-6 stimola il fegato a produrre epcidina, un ormone peptidico che agisce da regolatore chiave del metabolismo del ferro. L'epcidina, aumentando la sua sintesi, blocca efficacemente l'assorbimento del ferro a livello intestinale e ne inibisce il rilascio dai depositi cellulari, principalmente nei macrofagi. Questo sequestro di ferro rende il minerale meno disponibile per la sintesi dell'emoglobina, compromettendo l'eritropoiesi, ovvero la produzione di globuli rossi.
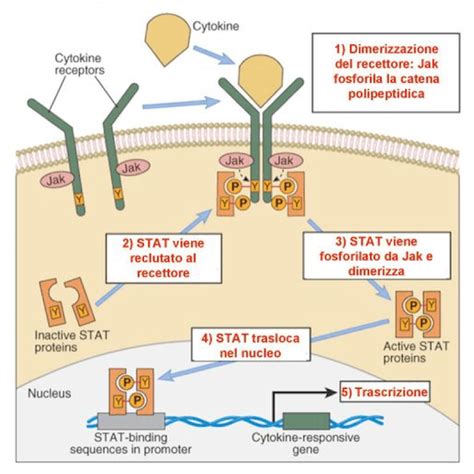
La sopravvivenza dei globuli rossi può essere leggermente ridotta a causa dell'aumentata emofagocitosi da parte dei macrofagi, un fenomeno più marcato in pazienti con malattie infiammatorie acute. L'eritropoiesi risulta insufficiente non solo per la ridotta disponibilità di ferro, ma anche per una ridotta sintesi di eritropoietina (EPO) e per una diminuita risposta del midollo osseo all'EPO stessa. Le citochine infiammatorie possono ulteriormente compromettere la proliferazione e la differenziazione delle cellule eritroidi, attraverso la formazione di radicali liberi e l'induzione dell'apoptosi (morte cellulare programmata). Il metabolismo del ferro è alterato in modo significativo a causa dell'aumento dell'epcidina, che inibisce sia l'assorbimento intestinale che il riciclaggio del ferro, portando a un suo sequestro. Le cellule reticolo-endoteliali sequestrano il ferro derivante dai globuli rossi invecchiati, rendendolo non disponibile per la sintesi dell'emoglobina e impedendo la correzione dell'anemia tramite un aumento della produzione di globuli rossi. Le citochine prodotte dai macrofagi in pazienti con infezioni, stati infiammatori e tumori contribuiscono alla riduzione della produzione di EPO e all'alterazione della disponibilità del ferro tramite la sintesi epatica aumentata di epcidina.
Effetti dei Trattamenti Oncologici: Chemioterapia e Radioterapia
La chemioterapia rappresenta una delle cause più frequenti di anemia iatrogena, ovvero indotta da interventi medici. Molti farmaci citotossici, progettati per colpire le cellule tumorali in rapida divisione, hanno come effetto collaterale la soppressione dell'attività del midollo osseo, un fenomeno noto come mielosoppressione. Questo danneggia non solo le cellule tumorali, ma anche le cellule staminali ematopoietiche sane, responsabili della produzione di tutte le cellule del sangue, inclusi i globuli rossi. Anche la radioterapia, specialmente se estesa a regioni corporee ricche di midollo osseo (come il bacino o la colonna vertebrale), può contribuire significativamente allo sviluppo dell'anemia, danneggiando le cellule ematopoietiche e compromettendo la loro capacità rigenerativa.
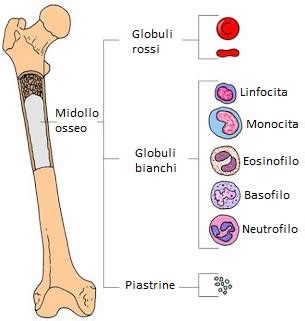
È importante sottolineare che il danno al midollo osseo indotto dai trattamenti oncologici è spesso temporaneo. Le pause tra i cicli di terapia consentono al midollo di rigenerarsi parzialmente, sebbene l'entità di questa rigenerazione possa variare. L'incidenza dell'anemia tende ad aumentare con il numero di cicli di trattamento chemioterapico somministrati.
Perdite Ematiche e Carenze Nutrizionali
I tumori che interessano il tratto gastrointestinale (stomaco, intestino, pancreas) o il sistema urogenitale sono frequentemente associati a sanguinamenti cronici, anche se di lieve entità e non sempre evidenti. Queste perdite ematiche continue possono condurre a un'anemia sideropenica, ovvero da carenza di ferro. I tumori del colon-retto, dello stomaco, del fegato, della cistifellea e delle vie biliari, del dotto pancreatico e del pancreas sono particolarmente inclini a causare queste perdite.
Inoltre, la malattia neoplastica stessa, o gli effetti dei trattamenti, possono portare a malnutrizione e carenze nutrizionali. La sensazione di malessere generalizzato, la nausea, la perdita di appetito e le alterazioni del gusto tipiche del paziente oncologico possono indurre una riduzione dell'apporto alimentare e una dieta non equilibrata. La carenza di micronutrienti essenziali come ferro, vitamina B12 e folati può ulteriormente aggravare o causare anemia. Più raramente, l'anemia può essere legata a insufficienza renale cronica, una condizione in cui i reni non riescono più a svolgere correttamente le loro funzioni, inclusa la produzione di eritropoietina.
Sintomatologia: Riconoscere i Segnali dell'Anemia
I sintomi dell'anemia nel paziente oncologico possono variare notevolmente in intensità, da lievi a gravemente debilitanti. La gravità dipende da diversi fattori, tra cui la velocità con cui l'anemia si sviluppa e la capacità intrinseca dell'organismo di compensare la ridotta ossigenazione dei tessuti.
Il sintomo cardine e più comunemente riferito è l'astenia, descritta dai pazienti come una stanchezza profonda, persistente e che non trova sollievo nel riposo. Questa fatica cronica ha un impatto devastante sulle attività quotidiane, compromettendo l'autonomia del paziente, la sua capacità di svolgere anche i compiti più semplici e incidendo pesantemente sul suo stato psicologico, favorendo ansia e depressione.
Altri sintomi comuni includono:
- Pallore cutaneo e mucoso: dovuto alla ridotta concentrazione di emoglobina, che conferisce il tipico colore rosso al sangue.
- Dispnea da sforzo: difficoltà respiratorie che si manifestano durante l'attività fisica, anche leggera, a causa della ridotta capacità del sangue di trasportare ossigeno.
- Tachicardia e cardiopalmo: il cuore aumenta la frequenza e la forza delle contrazioni per cercare di compensare la carenza di ossigeno, portando a palpitazioni e sensazione di battito accelerato.
- Vertigini e svenimenti: in casi di anemia più severa, la ridotta perfusione cerebrale può causare capogiri e, in casi estremi, episodi sincopali.
- Mal di testa: un sintomo aspecifico che può essere correlato alla ridotta ossigenazione cerebrale.
Va sottolineato che la presenza e l'intensità di questi sintomi sono strettamente legate alla velocità di insorgenza dell'anemia. Un'anemia che si sviluppa rapidamente, come nel caso di un'emorragia acuta, può manifestarsi con sintomi pronunciati anche con valori di emoglobina non eccessivamente bassi. Al contrario, un'anemia che progredisce lentamente e gradualmente può essere meglio tollerata, con sintomi lievi o addirittura assenti, permettendo all'organismo di adattarsi progressivamente.
ANEMIA: sintomi, cause e cosa fare🩸
Percorso Diagnostico: Identificare la Causa Sottostante
La diagnosi accurata e tempestiva dell'anemia nel paziente oncologico è essenziale per impostare un trattamento mirato e prevenire complicanze potenzialmente gravi. Il percorso diagnostico inizia con un'anamnesi dettagliata e un esame obiettivo approfondito, seguiti da una serie di esami di laboratorio specifici.
Esami di Laboratorio Fondamentali
- Emocromo Completo (CBC): Questo è l'esame di laboratorio primario. Permette di valutare il livello di emoglobina (Hb), il numero di globuli rossi (eritrociti) e l'ematocrito (la percentuale del volume sanguigno occupata dai globuli rossi). I valori al di sotto delle soglie di normalità (generalmente < 13 g/dL per gli uomini e < 12 g/dL per le donne, ma con variazioni in ambito oncologico) indicano la presenza di anemia. Si valutano anche indici eritrocitari come l'MCV (volume corpuscolare medio) e l'MCH (emoglobina corpuscolare media), che aiutano a classificare l'anemia in microcitica, normocitica o macrocitica.
- Conta dei Reticolociti: I reticolociti sono globuli rossi giovani, appena rilasciati dal midollo osseo. Un aumento della loro conta indica che il midollo osseo sta tentando di compensare l'anemia aumentando la produzione di nuovi eritrociti. Una conta bassa in presenza di anemia suggerisce una ridotta capacità del midollo osseo di produrre globuli rossi, come avviene in caso di mielosoppressione o infiltrazione midollare.
- Assetto Marziale: Questo pannello di esami è cruciale per valutare lo stato del ferro nell'organismo:
- Sideremia: Misura la quantità di ferro libero nel sangue.
- Ferritina sierica: Riflette i depositi totali di ferro nell'organismo. In condizioni di infiammazione cronica, la ferritina può essere elevata anche in presenza di carenza di ferro assoluta, agendo come proteina di fase acuta. Tuttavia, un valore di ferritina < 100 ng/mL in un paziente con infiammazione suggerisce fortemente una concomitante carenza di ferro.
- Transferrina e Saturazione della Transferrina (TSAT): La transferrina è la proteina che trasporta il ferro nel sangue. Una bassa saturazione della transferrina indica che il ferro disponibile è scarso. La TSAT è calcolata come rapporto tra sideremia e capacità totale di legare il ferro (legata alla transferrina).
- Recettore Solubile della Transferrina (sTfR): I livelli di sTfR aumentano in caso di carenza di ferro e sono utili per distinguere tra anemia da carenza di ferro e anemia da malattia cronica, soprattutto quando la ferritina è elevata a causa dell'infiammazione.
- Emoglobina Reticolocitaria (Ret-He): Misura la quantità di emoglobina presente nei reticolociti. Un valore basso indica una ridotta disponibilità di ferro per la sintesi dell'emoglobina, anche in presenza di livelli di ferro sierico normali.

Esami di Approfondimento
A seconda del sospetto clinico, possono essere necessari ulteriori accertamenti:
- Ricerca del Sangue Occulto nelle Feci: Fondamentale per identificare perdite ematiche gastrointestinali occulte.
- Endoscopie Digestive (Gastroscopia, Colonscopia): Utilizzate per visualizzare direttamente il tratto gastrointestinale e identificare la sede di eventuali sanguinamenti o lesioni tumorali.
- Dosaggio di Vitamina B12 e Folati: Per escludere o confermare carenze di queste vitamine, anch'esse importanti per l'eritropoiesi.
- Funzionalità Renale: Esami come creatinina e azotemia per valutare la funzionalità renale e l'eventuale impatto sulla produzione di EPO.
- Test di Emolisi: Se si sospetta un'anemia emolitica (distruzione accelerata dei globuli rossi), si possono eseguire test specifici come il test di Coombs.
Strategie Terapeutiche Personalizzate
Il trattamento dell'anemia nel paziente oncologico deve essere sempre personalizzato, tenendo conto della gravità dei sintomi, del tipo di tumore, dello stadio della malattia, degli obiettivi della cura oncologica e delle condizioni generali del paziente. Le principali opzioni terapeutiche includono:
Terapia Marziale (Ferro)
Se viene riscontrata una carenza di ferro, sia assoluta (bassi depositi) che funzionale (ferro non disponibile per l'eritropoiesi a causa dell'infiammazione), la somministrazione di ferro è un pilastro fondamentale del trattamento. Il ferro può essere somministrato per via orale o endovenosa.
- Ferro Orale: È la via di somministrazione più comune per le carenze lievi o moderate. Tuttavia, l'assorbimento del ferro orale può essere compromesso in pazienti oncologici a causa dell'infiammazione, della ridotta motilità intestinale o di precedenti interventi chirurgici. Inoltre, può causare effetti collaterali gastrointestinali come nausea, stipsi o diarrea.
- Ferro Endovenoso (EV): È spesso preferito nei pazienti oncologici, specialmente in quelli con anemia da malattia cronica, carenza funzionale di ferro, malassorbimento intestinale, o quando la terapia orale non è efficace o ben tollerata. Il ferro EV garantisce un ripristino più rapido ed efficace delle riserve di ferro e una migliore risposta all'eritropoiesi. Esistono diverse formulazioni di ferro EV, con profili di sicurezza e tollerabilità differenti.
Agenti Stimolanti l'Eritropoiesi (ESA)
Gli agenti stimolanti l'eritropoiesi (ESA), come l'eritropoietina alfa (EPO) e la darbepoetina alfa, sono farmaci che mimano l'azione dell'ormone naturale eritropoietina, stimolando il midollo osseo a produrre più globuli rossi. Sono indicati principalmente per i pazienti che sviluppano anemia a causa della chemioterapia, quando i livelli di emoglobina sono inferiori a una soglia definita (spesso < 10-10.5 g/dL) e in presenza di sintomi correlati all'anemia.
L'uso degli ESA deve essere attentamente valutato, poiché in alcuni studi sono stati associati a un aumento del rischio di eventi tromboembolici e, in contesti specifici, a un potenziale impatto negativo sulla sopravvivenza globale. L'efficacia degli ESA è spesso potenziata dalla concomitante somministrazione di ferro, specialmente in caso di carenza funzionale di ferro. La terapia con ESA viene generalmente interrotta quando i livelli di emoglobina tornano nella norma o si avvicinano a essa, o al termine del trattamento chemioterapico.
Trasfusioni di Sangue
La trasfusione di emazie concentrate rappresenta la strategia più rapida ed efficace per innalzare i livelli di emoglobina e correggere l'anemia grave. Viene generalmente riservata ai casi di anemia severa (Hb < 7-8 g/dL), quando il paziente presenta sintomi acuti e instabilità emodinamica, o quando altre terapie non sono sufficientemente rapide o efficaci. Le trasfusioni sono procedure sicure, ma comportano potenziali rischi, tra cui reazioni allergiche, trasmissione di infezioni (sebbene molto rara con i moderni screening), immunosoppressione e sovraccarico di ferro a lungo termine.
Approcci Terapeutici Innovativi e Supportivi
La gestione dell'anemia oncologica si avvale anche di un approccio globale che include:
- Nutrizione Adeguata: Un regime alimentare bilanciato e l'integrazione di vitamine e minerali sono cruciali per supportare l'eritropoiesi.
- Gestione dei Sintomi: Interventi mirati per alleviare la fatigue, come il counselling psicologico, la gestione dello stress e, se indicato, l'uso di farmaci antidepressivi o ansiolitici.
- Ottimizzazione della Terapia Oncologica: In alcuni casi, può essere opportuno modificare o sospendere temporaneamente la chemioterapia o la radioterapia se l'anemia compromette la tolleranza al trattamento o rende il paziente non candidabile a proseguire le cure. Questo aspetto, tuttavia, deve essere attentamente bilanciato con i potenziali rischi di una riduzione dell'efficacia terapeutica del tumore.
Prognosi e Implicazioni Cliniche
La prognosi dell'anemia nel paziente oncologico è strettamente legata alla risposta del tumore ai trattamenti. Se la neoplasia risponde bene alle cure e si ottiene un controllo della malattia, l'anemia tende a migliorare o a risolversi. Al contrario, un'anemia non trattata o refrattaria può portare a un deterioramento progressivo dello stato funzionale del paziente, rendendolo troppo debole per proseguire i cicli di chemioterapia programmati. Questo può avere un impatto negativo sulla sopravvivenza globale, poiché la riduzione della dose o la sospensione del trattamento chemioterapico possono compromettere l'efficacia della cura antitumorale.
La prevenzione dell'anemia neoplastica non è sempre possibile, essendo intrinsecamente legata alla biologia del tumore e alle sue interazioni con l'organismo ospite. Tuttavia, una diagnosi precoce, un monitoraggio attento e un trattamento tempestivo e personalizzato possono migliorare significativamente la qualità della vita del paziente, ottimizzare la tolleranza alle terapie oncologiche e, potenzialmente, influenzare positivamente la prognosi.
È fondamentale che il paziente oncologico comunichi tempestivamente al proprio oncologo o ematologo la comparsa di nuovi sintomi o il peggioramento di quelli esistenti, permettendo un intervento rapido e appropriato. La collaborazione tra il paziente, i familiari e il team medico è la chiave per una gestione efficace dell'anemia nel contesto oncologico.
tags: #anemia #nel #malato #oncologico

